Studiendesigns
Studienplanung
Experimentelle Studien werden nicht immer nach genau dem gleichen Prinzip durchgeführt. Es stehen verschiedene Studiendesigns zur Verfügung, die unterschiedliche Vor- und Nachteile mit sich bringen und nachfolgend vorgestellt werden. Eine Abwägung, welches Design am besten für das Untersuchungsvorhaben ist, sollte bereits vor Studienbeginn festgelegt und im Studienprotokoll dokumentiert werden. Es gibt kein in jedem Fall optimales Design und es sollten auch immer finanzielle und organisatorische Aspekte in die Entscheidung miteinbezogen werden.
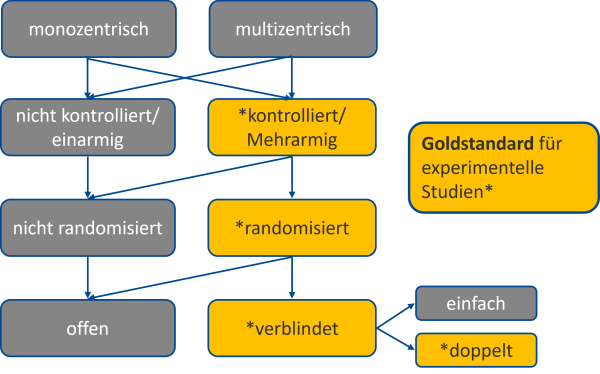
Die Übersicht rechts zeigt euch mögliche Studiendesigns, in denen die Methoden unterschiedlich miteinander kombiniert werden. In Gelb ist das Studiendesign einer doppelblinden RCT hervorgehoben, die wie gesagt den Goldstandard der experimentellen Forschung darstellt. Auch wenn doppelblinde RCTs Strukturgleichheit, Beobachtungsgleichheit und Behandlungsgleichheit garantieren, ist es wie bereits im Abschnitt zu den RCTs beschrieben, nicht immer möglich eine RCT durchzuführen und manchmal auch aus finanziellen und/oder organisatorischen Gründen nicht lohnenswert.
Zentrum
Die erste Frage, die sich stellt, ist ob die gesamte Studie oder die Datenerhebung innerhalb eines Forschungszentrums bzw. einer Forschungsinstitution (monozentrisch) oder Institutions-übergreifend (multizentrisch) erfolgen soll. Während es offensichtlich billiger und unkomplizierter ist, sich auf eine Forschungsstätte zu beschränken und die erhobenen Daten besser untereinander vergleichbar sind, kann durch ein multizentrisches Design einfacher die benötigte Anzahl an Studienteilnehmer:innen (siehe Fallzahlplanung) erreicht werden. Dies ist besonders bei seltenen Erkrankungen ein großer Vorteil. Außerdem kann durch die repräsentativere Stichprobe eine höhere externe Validität der Ergebnisse erreicht werden. Externe Validität bezeichnet die Übertragbarkeit oder Gültigkeit der Ergebnisse einer Studie auf eine andere Population oder eine andere Situation, was häufig Ziel wissenschaftlicher Studien ist (siehe Grundgesamtheit vs. Stichprobe).
Kontrolle
Als nächstes wird zwischen kontrollierten (oder mehrarmigen) und nicht kontrollierten (einarmigen) Studiendesigns unterschieden. Eine kontrollierte Studie vergleicht die Ergebnisse der Behandlungsgruppe mit denen einer sogenannten Kontrollgruppe, in der entweder gar keine Behandlung oder eine Behandlung mit der Standardtherapie, also der aktuellen Praxis, stattfindet. Die Kontrollgruppe dient als Vergleich zur Behandlungsgruppe und hilft, die Auswirkungen von Faktoren zu isolieren, die nicht Teil der betrachteten Intervention sind (z. B. dem natürlichen Krankheitsverlauf oder Veränderungen in der Umwelt). Ohne eine Kontrollgruppe ist es in der Regel nicht möglich, die Wirksamkeit einer Behandlung sicher zu beurteilen und klare Schlussfolgerungen über die Wirkung der Intervention zu ziehen.
Randomisierung
Wie verläuft nun aber die Verteilung der Versuchspersonen in die Interventions- und die Kontrollgruppe? Es wird unterschieden zwischen randomisierten und nicht randomisierten Studien. Die Zuteilung erfolgt in einer randomisierten Studie, wie der Name schon sagt, rein zufällig auf Basis eines vor Studienbeginn festgelegten zufälligen Prozesses (z. B. das Ziehen von zufälligen Zahlen etc). Randomisierung hilft, Merkmale, die das betrachtete Outcome beeinflussen könnten, gleichmäßig in beiden Gruppen zu verteilen. So wird sichergestellt, dass beide Gruppen eine ähnliche Merkmalszusammensetzung (Strukturgleichheit) aufweisen und dass die Unterschiede in den Outcomes auf die Intervention zurückzuführen sind, anstatt auf andere Faktoren. Somit ist Randomisierung ein wirksames Mittel gegen Confounding (siehe dazu Confounding, Bias und Co.) und damit verfälschte oder verzerrte Studienergebnisse.
Verblindung
Als letztes steht noch die Entscheidung darüber aus, wer über die verabreichte Therapie informiert ist und wer nicht. Ein offenes Studiendesign bedeutet, dass sowohl Studienteilnehmer:in als auch behandelnde Ärzt:innen über die Therapie Bescheid wissen, die sie erhalten bzw. verabreichen. Erfolgt eine einfache Verblindung, wird die Therapie entweder vor dem/der Studienteilnehmer:in (oder in besonderen Fällen vor dem/der behandelnden Ärzt:in) geheim gehalten. Dies kann z. B. mittels eines Placebos erfolgen, sodass Placebo- oder Noceboeffekte ausgeschlossen werden können. Ein Placeboeffekt beschreibt den Fall, dass der/die Patient:in durch ein positives Grundgefühl durch die erwartete Behandlung mit der neuen Therapie tatsächlich bessere Heilungschancen hat. Ein Noceboeffekt tritt im Gegensatz dazu ein, wenn durch die Scheinbehandlung negative Begleiterscheinungen, wie z. B. (eingebildete) Nebenwirkungen auftreten. Bei der doppelten Verblindung sind weder Ärzt:innen noch Studienteilnehmer:innen über die Behandlung informiert. Das beugt zusätzlich vor, dass der/die Ärzt:in mit seinen Erwartungshaltungen und dadurch beeinflusste Behandlung und/oder Beobachtung die Studienergebnisse, wenn auch unbewusst, verfälscht. Die doppelte Verblindung sichert also Behandlungsgleichheit und beugt so Behandlungsbias (die ungleiche Versorgung der Patient:innen im Studienverlauf) und Detektionsbias (die ungleiche Bewertung des/der betrachteten Endpunkte(s)) vor.
Beispiel "Blutdrucksenker"
In unserer Beispielstudie entscheiden wir uns für ein monozentrisches Design, denn es ist aufgrund einer relativ hohen Prävalenz unkompliziert, Patient:innen mit Bluthochdruck ausfindig zu machen und die finanziellen Ressourcen sind gering. Wir wollen außerdem das neue Medikament mit der Standardtherapie vergleichen, sodass wir eine Interventions- und Kontrollgruppe benötigen. Die Einteilung in die Gruppen kann ohne Probleme randomisiert werden. Da sowohl die Standardtherapie als auch das neue Medikament in optisch gleicher Tablettenform verabreicht werden können, kann auch ohne großen Aufwand eine Doppelverblindung stattfinden.
Es handelt sich somit in unserer Beispielstudie um eine monozentrische, kontrollierte, randomisierte und doppelt verblindete experimentelle Studie.
LITERATURVERZEICHNIS
Die Inhalte dieser Seite sind angelehnt an:
